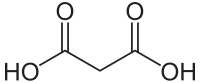
Malonsyre
Malonsyre er en dikarboksylsyre med kjemisk formel CH2(COOH)2. Ionisert form av malonsyre, slik som dets estere og salter, er kjent som malonater. For eksempel, dietylmalonat er malonsyres etyl ester. Navnet kommer fra Latin malum, som betyr eple.
| Malonsyre | |||||
|---|---|---|---|---|---|
| |||||
| Systematisk navn | |||||
| Propanediosyre | |||||
| Identifikatorer | |||||
| CAS-nummer | |||||
| Kjemiske egenskaper | |||||
| Formel | CH2(COOH)2 | ||||
| Molar masse | 104,061 g/mol | ||||
| Tetthet | 1619 kg/m3 | ||||
| Smeltepunkt | 135 - 137 °C | ||||
| Løselighet | 763 g/L | ||||
| pKa | pKa1 = 2,83 pKa2 = 5,69 | ||||
| Relatert | |||||
| Andre anioner | Malonat | ||||
Biokjemi
redigerKalsium saltet av malonsyre finnes i høye konsentrasjoner i rødbeter. Malonsyrens normaltilstand er som hvite krystaller.
Organisk syntese
redigerEn klassisk fremstilling av malonsyre starter fra eddiksyre. Denne syren blir klorert til kloreddiksyre. Natriumkarbonat danner natrium salt som så blir reagert med natriumcyanid til cyanoeddiksyresaltet i en nukleofil substitusjon. Nitril gruppen can bli hydrolysert med natriumhydroksid to natriummalonat og acidification affords malonsyre.
Organiske reaksjoner
redigerI en velkjent reaksjon inngår malonsyre i en kondensasjonsreaksjon med urea til barbitursyre. Malonsyre brukes ofte som enolat i Knoevenagel kondensasjoner eller kondenseres med aceton og danner Meldrums syre. Dets estere brukes også for -CH2COOH synton i malonestersyntese.
Patologi
redigerNår forhøyede malonsyrenivåer er ledsaget av forhøyede metylmalonsyrenivåer kan dette indikere den ofte uoppdagede [1] metabolske sykdommen kombinert malonsyre- og metylmalonsyreuri (CMAMMA). Ved å beregne ratioen mellom malonsyre og metylmalonsyre i plasma kan CMAMMA skilles fra klassisk metylmalonsyre-acidemi.[2]
Referanser
rediger- ^ NIH Intramural Sequencing Center Group; Sloan, Jennifer L; Johnston, Jennifer J; Manoli, Irini; Chandler, Randy J; Krause, Caitlin; Carrillo-Carrasco, Nuria; Chandrasekaran, Suma D; Sysol, Justin R (2011-09). «Exome sequencing identifies ACSF3 as a cause of combined malonic and methylmalonic aciduria». Nature Genetics. 9 (engelsk). 43: 883–886. ISSN 1061-4036. PMC 3163731 . PMID 21841779. doi:10.1038/ng.908. Sjekk datoverdier i
|dato=(hjelp) - ^ de Sain-van der Velden, Monique G. M. (2016). «A New Approach for Fast Metabolic Diagnostics in CMAMMA». I Morava, Eva. JIMD Reports, Volume 30. 30. Springer Berlin Heidelberg. s. 15–22. ISBN 978-3-662-53680-3. PMC 5110436 . PMID 26915364. doi:10.1007/8904_2016_531.
Kilder
rediger- (no) «Malonsyre» i Store norske leksikon
Eksterne lenker
rediger- (en) Malonic acid – kategori av bilder, video eller lyd på Commons
- pH spectrum https://web.archive.org/web/20170518231449/http://theoprax-research.com/ Disodium Malonate
- pH spectrum https://web.archive.org/web/20170518231449/http://theoprax-research.com/ Malonic acid copper complex