Ficks diffusjonslover
Ficks diffusjonslover beskriver diffusjon og ble avledet av Adolf Fick i 1855. De kan brukes til å løse diffusjonskoeffisienten, D. Ficks første lov kan brukes til å utlede ficks andre lov som igjen er identisk med diffusjonsligningen.
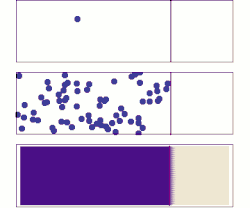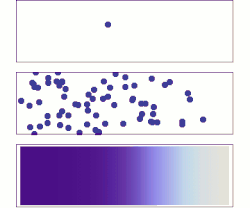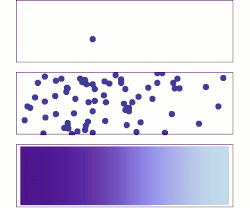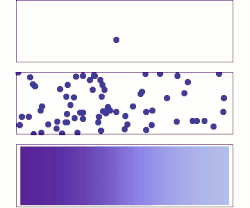
En diffusjonsprosess som overholder Ficks lover kalles normal eller Fickian diffusjon; en prosess som ikke overholder Ficks lover kalles anomal diffusjon eller ikke-fickian diffusjon.
Historie
redigerI 1855 var fysiolog Adolf Fick sin først rapporterte om sine nå kjente lover som regulerer transport av masse gjennom diffusive midler. Ficks arbeid ble inspirert av de tidligere eksperimentene til Thomas Graham, som ikke la opp til å foreslå de grunnleggende lovene som Fick skulle bli kjent for. Ficks lov er analog med forholdene som ble oppdaget i samme epoke av andre fremtredende forskere: Darcys lov (hydraulisk strømning), Ohms lov (ladningstransport) og Fouriers lov (varmetransport).
Ficks eksperimenter (modellert etter Grahams) handlet om å måle konsentrasjonene og saltstrømmene, diffundere mellom to reservoarer gjennom vannrør. Det er bemerkelsesverdig at Ficks arbeid primært gjaldt diffusjon i væsker, fordi diffusjon i faste stoffer på det tidspunktet ikke ble ansett som generelt mulig. I dag danner Ficks lover kjernen i vår forståelse av diffusjon i faste stoffer, væsker og gasser (i fravær av bulk væskebevegelse i de to sistnevnte tilfellene). Når en diffusjonsprosess ikke følger Ficks lover (som skjer i tilfeller av diffusjon feks. gjennom porøse medier), blir det referert til som ikke-Fickian.
Ficks første lov
redigerFicks første lov relaterer den diffusive fluksen til konsentrasjonsgradienten. Det postulerer at fluksen går fra regioner med høy konsentrasjon til regioner med lav konsentrasjon, med en størrelse som er proporsjonal med konsentrasjonsgradienten (romlig derivat), eller i forenklede termer konseptet at en løsemiddel vil bevege seg fra et område med høy konsentrasjon til et område med lav konsentrasjon over en konsentrasjonsgradient. I en (romlig) dimensjon kan loven skrives i forskjellige former, hvor den vanligste formen (se ) er på molar basis:
hvor
- J er diffusjonsstrømmen, hvor dimensjonen er mengden stoff per arealeenhet per tidsenhet. J måler mengden stoff som vil strømme gjennom et enhetsareal i løpet av et tidsintervall.
- D er diffusjonskoeffisienten eller diffusiviteten. Dimensjonen er areal per tidsenhet.
- φ (for ideelle blandinger) er konsentrasjonen, der dimensjonen er mengden stoff per volumsenhet.
- x er posisjon, hvis dimensjon er lengde.
D er proporsjonal med den kvadratiske hastigheten til de diffuserende partiklene, som avhenger av temperaturen, viskositeten til væsken og størrelsen på partiklene i henhold til forholdet Stokes–Einstein. I fortynnede vandige løsninger er diffusjonskoeffisientene til de fleste ioner like og har verdier som ved romtemperatur er i området (0.6-2) x 10−9 m2/s. For biologiske molekyler varierer diffusjonskoeffisientene normalt fra 10−11 til 10−10 m2/s.
I to eller flere dimensjoner må vi bruke ∇, nabla- eller gradientoperatøren, som generaliserer det første derivatet, oppnår
hvor J betegner diffusjonsfluksvektoren.
Drivkraften for den endimensjonale diffusjonen er mengden −∂φ/∂x, som for ideelle blandinger er konsentrasjonsgradienten.
Alternative formuleringer av den første loven
redigerEn annen form for den første loven er å skrive den med den primære variabelen som massefraksjon(yi,gitt for eksempel i kg/kg), deretter endres ligningen til:
hvor
- indeksen i betegner ith-spesiet,
- Ji er diffusjonsfluksvektoren til ith-speciet (for eksempel i mol/m2-s),
- Mi er molarvekten til ith-spesiet, og
- ρ er blandingstettheten (for eksempel ikg/m3).
Bemerk at er utenfor gradientoperatøren. Dette er fordi:
hvor ρsi er den delvise tettheten til ith spesiet.
Utover dette, i andre kjemiske systemer enn ideelle løsninger eller blandinger, er drivkraften for diffusjon av hvert spesie gradienten av det kjemiske potensialet til dette spesiet. Da kan Ficks første lov (endimensjonal tilfelle) skrives
hvor
- indeksen i betegner ith spesiet.
- c er konsentrajonen (mol/m3).
- R er den universelle gasskonstanten (J/K/mol).
- T er den absolutte temperaturen (K).
- µ er det kjemiske potensialet (J/mol).
Drivkraften til Ficks lov kan uttrykkes som en flyktighetsforskjell:
Flyktighet har Pa enhet. er et delvis trykk av komponent i i damp eller væske fase. Ved dampvæskevekt er fordampningsstrømmen null fordi .
Utledning av Ficks første lov for gasser
redigerFire versjoner av Ficks lov for binære gassblandinger er gitt nedenfor. Disse antar: termisk diffusjon er ubetydelig; kroppskraften per masseenhet er den samme på begge spesier; og enten trykk er konstant, eller begge spesier har samme molare masse. Under disse forholdene viser i detalj hvordan diffusjonsligningen fra den kinetiske teorien om gasser reduseres til denne versjonen av Ficks lov:
,
hvor Vi er diffusjonshastigheten til spesiet i. Når det gjelder spesiefluxen, er dette
.
Hvis i tillegg, , dette reduseres til den vanligste formen for Ficks lov,
.
Hvis (i stedet for eller i tillegg til ) begge spesiene har samme molare masse, blir Ficks lov
,
hvor er molfraksjonen av spesiet i.
Ficks andre lov
redigerFicks andre lov forutsier hvordan diffusjon får konsentrasjonen til å endres med hensyn til tid. Det er en delvis differensialligning som i en dimensjon lyder:
hvor
- er konsentrasjonen i dimensjoner på [(stoffmengde) lengde−3],for eksempel i mol/m3; = (x,t) er en funksjon som avhenger av plassering x og tid t
- t er tid, for eksempel s
- Der diffusjonskoeffisienten i dimensjoner på [lengde2 tid−1], for eksempel m2/s
- x er posisjonen [lengde], for eksempel m
I to eller flere dimensjoner må vi bruke Laplacian Δ = ∇2, som generaliserer det andre derivatet og oppnår ligningen
Ficks andre lov har samme matematiske form som varme-ligningen, og dens grunnleggende løsning er den samme som varme-kjernen, bortsett fra å bytte termisk ledningsevne med diffusjonskoeffisient :
Applikasjoner av Ficks lov
redigerLigninger basert på Ficks lov har ofte blitt brukt til å modellere transportprosesser i matvarer, nevroner, biopolymerer, legemidler, porøs jord, populasjonsdynamikk, kjernefysiske materialer, plasmafysikk og dopingprosesser av halvledere. Teorien om voltammetriske metoder er basert på løsninger av Ficks ligning. På den annen side er en "Fickian" -beskrivelse i noen tilfeller utilstrekkelig. For eksempel i polymervitenskap og matvitenskap er det nødvendig med en mer generell tilnærming for å beskrive transport av komponenter i materialer som gjennomgår en glassovergang. Et mer generelt rammeverk er Maxwell-Stefans diffusjonsligning for flerkomponentmasseoverføring, der Ficks lov kan oppnås som et begrensende tilfelle, når blandingen er ekstremt fortynnet og hvert kjemisk spesie samhandler bare med bulkblandingen og ikke med andre spesier. For å redegjøre for tilstedeværelsen av flere spesier i en ikke-fortynnet blanding, brukes flere varianter av Maxwell-Stefan-ligningene. Se også ikke-diagonale koblede transportprosesser (Onsager-forhold).
Se også
redigerLitteratur
rediger- Smith, W. F. (2004). Foundations of Materials Science and Engineering (3rd utg.). McGraw-Hill.
- Berg, H. C. (1977). Random Walks in Biology. Princeton.
- Bird, R. B.; Stewart, W. E.; Lightfoot, E. N. (1976). Transport Phenomena. John Wiley & Sons.
- Crank, J. (1980). The Mathematics of Diffusion. Oxford University Press.
- Bokshtein, B. S.; Mendelev, M. I.; Srolovitz, D. J., red. (2005). Thermodynamics and Kinetics in Materials Science: A Short Course. Oxford: Oxford University Press. s. 167–171.
- Fick, A. (1855). «On liquid diffusion». Annalen der Physik und Chemie. 94: 59.