Knallkvikksølv
Knallkvikksølv eller kvikksølvfulminat er et stoff med kjemisk formel Hg(CNO)2. Stoffet er et fast, gråbrunt krystallisk pulver. Knallkvikksølv er eksplosivt i luft, men når det oppbevares under vann er det stabilt. Tørt knallkvikksølv er følsomt for sjokk, friksjon og varme. Ved antenning deflagrerer stoffet raskt og spaltes til kvikksølvdamp, karbonmonoksid og nitrogengass
| Knallkvikksølv | |||
|---|---|---|---|
 | |||
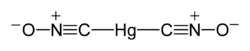 | |||
| Andre navn | |||
| Kvikksølvfulminat | |||
| Identifikatorer | |||
| CAS-nummer | |||
| Kjemiske egenskaper | |||
| Formel | Hg(CNO)2 | ||
| Molar masse | 285,96662 g/mol | ||
| Utseende | Fast, gråbrunt krystallisk pulver | ||
| Tetthet | 4420 kg/m3 | ||
| Smeltepunkt | 160 °C | ||
| Kokepunkt | 356,6 °C | ||
| Løselighet | Såvidt løselig | ||
| Farer | |||
| Hovedfarer | Svært giftig, følsomt for støt, Eksplosivt | ||
| Tenntemperatur | 170 °C | ||
- Hg(CNO)2 → Hg + 2CO + N2
Fremstilling
redigerKnallkvikksølv fremstilles ved å først reagere kvikksølv med konsentrert salpetersyre og deretter tilsette etanol. Det ble første gang framstilt i år 1800 av Edward Charles Howard.[1]
Egenskaper og bruksområder
redigerKnallkvikksølv vil begynne å dekomponere[klargjør] ved omkring 100 °C, men overskuddsvarmen fra reaksjonen vil fort øke temperaturen til dekomponeringen blir eksplosiv, derav navnet «knallkvikksølv». Dekomponering kan også skje ved fysisk påvirkning, for eksempel gjennom et slag fra en metallgjenstand.[2] Stoffet ble tidligere brukt i tennhetter til patroner og i eldre tid til kruttlapper og andre friksjonsbaserte sprengmidler. Stoffet er nå tatt ut av bruk på grunn av stoffets giftige egenskaper og siden produktene også er giftige og miljøfarlig
Referanser
rediger- ^ Edward Howard (1800). «On a New Fulminating Mercury». Philosophical Transactions of the Royal Society of London. 90 (1): 204–238. doi:10.1098/rstl.1800.0012.
- ^ W. E. Garner & H. R. Hailes (1933). «Thermal decomposition and detonation of mercury fulminate» (PDF). Proceedings of the Royal Society of London. 139 (1–3): 1–40. Bibcode:1933CP....334..128S. doi:10.1098/rspa.1933.0040. Arkivert fra originalen (PDF) . Besøkt 11. mars 2013.